Retour au format normal
Acide-Base : Diagnostic des acidoses métaboliques
Premičre publication : septembre 1999
Mise en ligne : 5 octobre 2001par
Objectifs
Savoir définir une acidose métabolique et connaître les principales complications associées
Connaître la démarche diagnostique devant une acidose métabolique
Connaître les principales causes d’acidose métabolique et leurs caractéristiques diagnostiques
Evaluation diagnostique des acidoses métaboliques
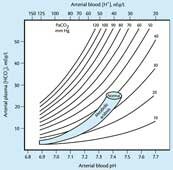
L’évaluation d’un patient avec une diminution de la concentration plasmatique de bicarbonate doit commencer par la réalisation de gaz du sang artériels pour exclure une hyperventilation primitive. L’acidose métabolique est définie par une augmentation de la concentration des protons au-dessus de 42 nmol/l ou un abaissement du pH en-dessous de 7,38. L’acidose est dite "métabolique" si la concentration de bicarbonates plasmatiques est abaissée en-dessous de 22 mmol/l. La PCO2 s’abaisse secondairement par compensation ventilatoire. L’évaluation du degré de compensation ventilatoire est importante pour apprécier la possibilité d’un trouble acido-basique complexe. Normalement, la diminution de PCO2 compensatoire est d’environ 1,2 mmHg pour chaque baisse de 1 mmol de la concentration plasmatique en bicarbonates. Si la PCO2 est significativement plus basse ou plus élevée que cette valeur, alors il faut suspecter respectivement une alcalose ou une acidose respiratoire associée. Le diagnostic peut être encore plus compliqué chez des patients ayant des désordres complexes au cours desquels l’acidose métabolique est le composant le moins marqué. Ces cas peuvent généralement être évoqués avec une reconstitution soigneuse de l’histoire clinique et la comparaison de la chute des bicarbonates plasmatiques avec l’augmentation du trou anionique (rapportdCO3/dTA).
voir la figure Compensation rrespiratoire de l’acidose métabolique : intervalles de confiance des variations de pH, bicarbonatémie, PCO2
La détermination du trou anionique plasmatique est la deuxième étape importante dans le diagnostic de l’acidose métabolique.
Le trou anionique plasmatique représente la différence entre les cations mesurés et les anions mesurés. Dans la mesure où le sodium est le principal cation mesuré et le chlore et les bicarbonates les principaux anions mesurés, le trou anionique équivaut à :TA = [Na] - [ Cl] - [HCO3]
Chez le sujet normal, le trou anionique est principalement déterminé par les charges négatives présentes sur les protéines plasmatiques et en particulier l’albumine. Il en résulte que la valeur attendue du trou anionique doit être ajustée vers le bas chez les patients hypoalbuminémiques (le trou anionique diminue d’environ 2,5 mmol/l pour chaque diminution de 10 g/l d’albuminémie).
Les valeurs normales du trou anionique plasmatique ont longtemps été de 7 à 13 mmol/l. Cependant, avec le recours aux nouveaux auto-analyseurs qui retrouvent des concentrations plus élevées de chlore, le trou anionique normal n’est plus que de 3 à 11 mmol/l et ces valeurs doivent donc être interprétées en fonction des normes du laboratoire local de référence. Une augmentation artéfactuelle du trou anionique peut être induite par une diminution des cations non mesurés notamment calcium et magnésium ou plus fréquemment par une augmentation des anions non mesurer comme notamment une hyperalbuminémie liée à une contraction volémique ou l’accumulation d’un anion organique en cas d’acidose métabolique.
voir la figure Représentation schématique du trou anionique et des acidoses hyper- ou normochlorémiques"
Dans une acidose métabolique où l’excès d’acide est tamponné par un bicarbonate extracellulaire, le bicarbonate est remplacé sur une base équimolaire par le chlore et il n’y a pas de modification du trou anionique. L’acidose métabolique est dite "hyperchlorémique" en raison de l’augmentation de la concentration plasmatique de chlore.
Une situation similaire s’observe au cours de la diarrhée et de l’acidose tubulaire proximale aboutissant à la perte de bicarbonate. Le rein compense en retenant du chlorure de sodium pour préserver le volume extracellulaire, l’effet net étant un remplacement mmol par mmol du bicarbonate par du chlorure. De façon analogue, l’acidose tubulaire distale et l’hypoaldostéronisme s’accompagnent d’une acidose à trou anionique normal et en raison de l’absence de rétention d’anions non mesurés.
Lorsque l’acidose est liée à l’accumulation d’un proton combiné à un anion peu ou pas métabolisé, l’accumulation de cet anion non mesuré augmente le trou anionique. L’acidose est bien liée à l’accumulation de protons mais l’anion indosé non métabolisé devient alors un outil diagnostique précieux.
Les principales causes d’acidose métabolique avec trou anionique élevé sont :
- l’acidose lactique habituellement liée à une hypoperfusion systémique marquée ou un cancer.
- Une acidocétose liée à un diabète, à l’alcool ou le jeûne ; situations au cours desquelles l’accumulation de béta-hydroxy-butyrate est le principal anion non mesuré.
- La plupart des patients en insuffisance rénale au cours de laquelle il y a rétention à la fois de protons et d’anions, comme les sulfates, phosphates et urates.
- Les ingestions au cours desquelles l’anion principal accumulé est le formate avec le méthanol, le glycolate et l’oxalate avec l’éthylène-glycol, les cétones et lactates avec l’aspirine. Cependant le trou anionique peut être normal au cours des intoxications par le méthanol ou l’éthylène-glycol s’il y a en même temps une ingestion d’alcool : celui-ci est en compétition avec l’alcool-déshydrogénase, diminuant le métabolisme du méthanol ou de l’éthylène-glycol en ses métabolites toxiques.
D’une façon générale, l’utilité diagnostique d’un trou anionique augmenté est plus importante lorsque le trou anionique dépasse 25 mmol/l. Dans ce cas, l’une des conditions citées précédemment est pratiquement toujours présente. Inversement, il n’est pas toujours possible d’identifier les anions non mesurés pour des élévations plus faibles du trou anionique en particulier lorsque celui-ci est inférieur à 20 mmol/l. L’augmentation de la concentration d’albumine, de phosphates peut contribuer mais d’autres anions moins facilement identifiables peuvent également être présents.
Enfin, il est possible d’observer un chevauchement entre des acidoses métaboliques responsables de trous anioniques normaux ou élevés.
La diarrhée par exemple est habituellement associée à un trou anionique normal. Dans certains syndromes cholériformes sévères cependant, le trou anionique peut être augmenté en raison de l’acidose lactique induite par l’hypoperfusion, l’hyperalbuminémie induite par la contraction volémique et enfin l’hyperphosphatémie de transfert liée à l’acidose.
Inversement, l’acidocétose diabétique est habituellement associée à un trou anionique élevé. Si la fonction rénale se maintient ainsi que le volume extracellulaire, une grande partie des anions cétoniques en excès peut être excrétée dans l’urine sous forme de sels de sodium ou de potassium. Dans ce cas, l’augmentation du trou anionique peut être bien moindre que celle attendue compte tenu de la sévérité de l’acidose métabolique. De plus, la perte urinaire de ces anions organiques est équivalente à la perte de bicarbonates puisque le métabolisme des anions cétoniques aboutit à la régénération de bicarbonates.
Des constatations analogues peuvent s’appliquer à l’acidose D-lactiques et à l’acidose métabolique induite par le toluène au cours de laquelle le trou anionique peut être soit élevé (accumulation de D-lactate et d’hippurate respectivement) ou au contraire normal en raison de l’élimination urinaire rapide des anions excessifs non mesurés.

voir la figure Causes des acidoses métaboliques.
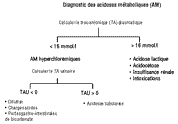
voir la figure Approche diagnotique d’une acidose métabolique
2. Diagnostic étiologique et physiopathologique des acidoses métaboliques
Les anions organiques ingérés ou générés par le métabolisme ont 2 devenirs possibles : l’addition initiale d’un acide organique au plasma aboutit à la titration du bicarbonate et à la génération d’un sel de sodium de cet anion dans le plasma. Certains anions organiques, comme l’acétoacétate, le béta-hydroxy-butyrate ou le lactate sont facilement métabolisés en bicarbonates et il n’y a donc pas de modification nette de la concentration plasmatique en bicarbonates. Cependant l’excrétion urinaire de ces anions organiques sous forme de sels de sodium produit une perte nette de bicarbonate de sodium et par conséquent une acidose hyperchlorémique. Au cours de tous ces désordres aboutissant à une acidose métabolique avec une augmentation du trou anionique, l’acide organique est ingéré ou généré plus rapidement qu’il ne peut être métabolisé ou excrété aboutissant à la fois à une perte nette de bicarbonates et à l’accumulation du sel de sodium de cet acide dans le plasma. Les 3 voies métaboliques ne sont pas mutuellement exclusives. Ainsi au cours de l’acidocétose diabétique, l’accumulation et l’excrétion des anions cétoniques prédominent mais après traitement, le métabolisme est la principale voie d’élimination.
Les sources les plus fréquentes d’acide organique endogène sont le béta-hydroxy-butyrate et l’acéto-acétate au cours de l’acidocétose, le lactate dans l’acidose lactique, et les acides organiques qui s’accumulent au cours de l’insuffisance rénale sévère (acides aliphatiques dicarboxyliques, acides phénoliques aromatiques, acide furanoique, acide 3-carboxy-4-méthyl-5-propyl-2-furane-propionique et acide hippurique). La rétention de ces anions organiques survient seulement au cours des maladies rénales très avancées et est pratiquement toujours précédée par une phase d’acidose hyperchlorémique. L’anion organique le plus fréquemment rencontré par ingestion et métabolisme sont les salycilates, le glycolate, le glyoxalate et l’oxalate, tous provenant du métabolisme de l’éthylène-glycol, et le formate provenant du métabolisme du méthanol.
Les acides cétoniques, lactates, salycilates, méthanol et éthylène-glycol sont facilement mesurables et quantifiables par la plupart des laboratoires cliniques. L’ingestion d’éthylène-glycol ou de méthanol est habituellement associée à une augmentation du trou osmolaire plasmatique et l’éthylène-glycol produit une cristallurie d’oxalate de calcium. Dans les désordres liés entièrement à l’accumulation d’anions non-mesurés, la réduction de la concentration en bicarbonates plasmatiques correspond exactement au trou anionique. Si cela n’est pas le cas, un deuxième désordre acidebase (acidose hyperchlorémique ou alcalose métabolique) peut être associé. Lorsqu’une alcalose et une acidose métabolique coexistent par exemple au cours du vomissement et de l’acidocétose, la concentration plasmatique en bicarbonates peut être normale et l’augmentation du trou anionique peut être le seul élément initial d’une anomalie acido-basique sous-jacente.
L’acidose hyperchlorémique est une conséquence de la rétention nette d’HCl ou d’un équivalent métabolique (par exemple le chlorure d’ammonium et les sels chlorés d’amino-acides) ou une perte de bicarbonate de sodium ou son équivalent métabolique (excrétion de sel ou d’anion organique en excès proportionnel de chlore). Dans le plasma normal, le rapport bicarbonate/chlore est largement supérieur à 0,25. La perte de bicarbonates peut survenir soit par le tube digestif en raison de diarrhées ou de fistule biliaire par exemple ou soit par excrétion rénale de bicarbonates ou leur équivalent ou en raison d’une génération rénale de bicarbonate insuffisante pour compenser un apport alimentaire ou une production d’acide.
Les causes rénales de perte de bicarbonate peuvent être distinguées des causes non rénales par la mesure de l’ammoniurie. Au cours de l’acidose hyperchlorémique, une excrétion urinaire quotidienne d’ammonium inférieure à 1 mmol/kg est anormale et indique que le rein est la cause principale de cette anomalie. Si la mesure de l’ammoniurie n’est pas facilement disponible, celle-ci peut être estimée à partir du trou anionique urinaire : TAU : UNa + UK - UCl
Un TAU > 0 signe l’origine tubulaire rénale de l’acidose alors qu’un TAU < 0 signe l’origine extrarénale de l’acidose. Si le pH urinaire est > à 6,5 il faut mesurer UHCO3 et l’inclure dans l’équation. L’équation n’est pas utilisable en présence dans l’urine d’anions non réabsorbables.
a) acidose métabolique avec augmentation de l’ammoniurie :
- Les pertes gastrointestinales de bicarbonates à partir d’aspiration digestive ou de diarrhée produisent une acidose hyperchlorémique si la vitesse de perte en bicarbonates excède les capacités de régénération rénale des bicarbonates. Une perte effective de bicarbonate peut également survenir de l’injection d’un acide organique avec une perte associée d’un sel de sodium et de potassium dans les selles.
- La génération de grandes quantités d’anions organiques produit une acidose hyperchlorémique si l’excrétion de l’anion est suffisamment rapide pour empêcher l’accumulation des anions dans le plasma. Les principales causes comprennent l’acétonurie (par exemple au cours de la phase de récupération d’une acidocétose diabétique), une acidurie hippurique provenant du métabolisme du toluène ("glue sniffing" ou inhalation de colle) ou d’une acidurie D-lactate dans le syndrome de l’anse intestinale borgne.
- L’administration de chlorure d’ammonium ou de sel chloré d’amino-acide produit une acidose hyperchlorémique en raison de leur métabolisme en l’HCl.
- L’administration d’autres sels chlorés peut également produire une acidose de dilution lorsqu’il existe une rétention franche du chlore comme par exemple au cours d’une déplétion volémique du liquide extracellulaire, l’insuffisance cardiaque ou après l’administration rapide de solutés salés isotoniques par voie intraveineuse.
b) Acidose métabolique avec ammoniurie abaissée (inappropriée)
Les anomalies de la régénération rénale ou de la réabsorption de bicarbonate sont les principales causes d’acidose hyperchlorémique avec réduction de l’excrétion urinaire d’ammoniurie. Ces acidoses tubulaires rénales peuvent être distinguées sur la base des variations du pH urinaire en réponse aux modifications de la bicarbonatémie. Le pH urinaire est inférieur ou égal à 6 pour une bicarbonatémie normale à 24 mmol/l et la baisse de la bicarbonatémie induit une réduction progressive du pH urinaire
- Acidose distale de type 1
Dans cette forme d’acidose tubulaire, la sécrétion de protons dans le tube collecteur ou la capacité à abaisser le pH urinaire est altérée. Le pH urinaire ne peut diminuer en-dessous de 5 même en présence d’une acidose métabolique sévère. L’administration de furosémide réduit le pH urinaire en-dessous de 5,5 chez des sujets normaux mais pas chez des patients avec une acidose tubulaire de type 1. La PCO2 urinaire ou plus exactement le gradient de PCO2 (deltaPCO2) entre l’urine et le sang dans une urine alcaline qui représente un index de sécrétion de proton dans le tube collecteur est souvent anormal au cours de cette forme d’acidose tubulaire distale.
Plusieurs sous-types d’acidose tubulaire distale ont été identifiés. Certains patients ont un tube collecteur excessivement perméable aux protons (défaut de gradient ou de perméabilité) comme c’est le cas au cours de l’administration d’amphotéricine B avec une PCO2 urinaire normale dans une urine alcaline.
Chez les patients avec un débit sécrétoire de protons anormalement bas (défaut sécrétoire) la PCO2 urinaire est anormalement basse. Cette forme est généralement associée à une hypokaliémie sévère car la réabsorption de sodium dans le tube collecteur s’accompagne d’une sécrétion de potassium plutôt que celle de protons. Les principales causes de ces anomalies sont le déficit en anhydrase carbonique de type 2, des mutations du gène codant pour la protéine de transport anionique AE1, et des défauts de la proton-ATPase du tube collecteur comme au cours du syndrome de Sjögren.
Les patients ayant une différence de potentiel anormalement basse dans le tube collecteur (défaut de potentiel) ont également une PCO2 urinaire basse mais la kaliémie est habituellement normale, voire élevée et l’excrétion urinaire de potassium reste basse après administration de furosémide. L’acidose tubulaire distale par défaut de potentiel est observée au cours des obstructions de l’arbre urinaire, des néphropathies interstitielles associées au lupus érythémateux et surtout avec l’administration de diurétiques dits épargneurs du potassium, tel que l’amiloride (Modamide®) ou triamtérène (Teriam®).
Dans la forme incomplète d’acidose tubulaire distale, la capacité maximale d’acidification de l’urine est altérée alors que la concentration plasmatique de bicarbonates reste normale. Ces patients se présentent cliniquementavec des lithiases urinaires et/ou une néphrocalcinose. La cause en est liée au pH urinaire alcalin, à l’hypercalciurie secondaire à l’acidose et à une concentration urinaire de citrates abaissée, le citrate étant un important inhibiteur de la cristallisation d’oxalate de calcium dans l’urine.
- Acidose tubulaire proximale de type 2
L’anomalie de la réabsorption proximale de bicarbonates aboutit à augmenter le débit de bicarbonate délivré dans le tube collecteur en excès de sa capacité de réabsorption. Après une bicarbonaturie initiale, la concentration plasmatique de bicarbonate et la quantité de bicarbonate filtré diminuent tous deux et un nouvel état d’équilibre est atteint en quelques heures avec une acidose hyperchlorémique et une urine totlement dépourvue en bicarbonate. Le pH urinaire est généralement acide (selon l’alimentation). La suspiçion d’acidose tubulaire proximale est confirmée par la bicarbonaturie significative (pH urinaire supérieur à 6,5) en présence d’un taux de bicarbonate plasmatique abaissé. Ceci peut être évalué facilement par l’administration orale ou intraveineuse de bicarbonate et un prélèvement de bicarbonate plasmatique lorsque le pH urinaire est supérieur à 6,5. Une concentration plasmatique de bicarbonate inférieure à 22 mmol/l, témoin d’un seuil réduit de réabsorption du bicarbonate, confirme le diagnostic. La mesure de la fraction d’excrétion de bicarbonate peut confirmer le diagnostic d’acidose tubulaire proximale mais la réalisation en est plus compliquée. La PCO2 urinaire en urine alcaline est habituellement supérieure à 65 mmHg dans l’acidose tubulaire proximale mais peut être réduite en cas d’atteinte distale associée, comme par exemple dans le déficit en anhydrase carbonique de type 2.
L’acidose tubulaire proximale peut survenir comme une anomalie isolée du transport du bicarbonate. Le plus souvent cependant, l’’acidose tubulaire proximale survient dans le cadre d’un syndrome de Fanconi associant plusieurs anomalies de transport dans le tube proximal et peut être causée par une néphropathie myélomateuse à chaines légères, des toxiques rénaux et certaines maladies génétiques. L’excrétion urinaire de citrate peut être normale au cours de l’acidose tubulaire proximale mais est abaissée par l’administration de chlorure d’ammonium.
- Ammoniogénèse défectueuse (acidose tubulaire distale hyperkaliémique de type 4)
Une production insuffisante d’ammoniaque induit une acidose tubulaire de type 4. La capacité à réabsorber le bicarbonate et acidifier l’urine est préservée mais la quantité d’acide excrétée est réduite en raison d’une insuffisance de tampon urinaire et d’autre part la génération de bicarbonate dans le tube collecteur est insuffisante pour préserver le bilan acide-base.
L’ammoniogénèse peut être altérée par la suppression physiologique de l’hyperkaliémie ou de l’insuffisance en glucocorticoïdes. L’hyperkaliémie déprime la production rénale d’ammoniaque, probablement en inhibant la sortie de bicarbonate de la cellule tubulaire proximale et en augmentant le pH intracellulaire. L’acidose tubulaire de type 4 au cours de l’insuffisance en minéralocorticoïde provient de la suppression de la production d’ammoniaque par l’hyperkaliémie. Les glucocorticoïdes sont nécessaires à la fois à l’augmentation du catabolisme protéique musculaire squelettique, à la synthèse de la glutamine et à la stimulation de l’ammoniogénèse rénale observée au cours de l’acidose métabolique. La perte d’une masse rénale fonctionnelle suffisante altère l’ammoniogénèse en diminuant le nombre de cellules tubulaires proximales générant l’ammoniaque. L’acidose tubulaire de type 4 n’est habituellement pas observée avant que 70 à 80 % des néphrons ne soient perdus mais avant ce stade des situations hypercataboliques au cours desquelles la génération de protons augmente (fièvre, maladie intercurrente sévère, administration de glucocorticoïdes, hyperalimentation) peuvent induire une acidose franche. Dans certaines maladies rénales, notamment les obstructions de l’appareil urinaire, la production rénale d’ammoniaque est déprimée même s’il n’y a pas de perte substantielle de la masse fonctionnelle rénale. Dans ce cas, les anomalies de l’architecture tubulo-interstitielle du néphron altèrent la capacité de réabsorption du NH3 dans l’anse de Henle et son accumulation dans la médullaire rénale.

voir la figure Principales caractéristiques des acidoses tubulaires

voir la figure Approche diagnostique des acidoses tubulaires
3. Traitement des acidoses métaboliques
3.1 Acidoses métaboliques aiguës
L’acidose métabolique aiguë sévère (définie par un pH < 7,10 et une bicarbonatémie < 8 mmol/l en présence d’une compensation respiratoire adéquate) est une situation grave mettant en jeu le pronostic vital en raison de multiples complications potentielles résumées dans le tableau 2.
Tableau 2 : Principales conséquences cliniques de l’acidémie sévère
- Cardiovasculaire
o Diminution de la contractilité cardiaque
o Augmentation de la résistance vasculaire pulmonaire
o Réduction du débit cardiaque, hépatique et rénal
o Hypotension artérielle
o Sensibilisation aux arythmies par réentrée et abaissement du seuil de fibrillation ventriculaire
o Atténuation de la réponse cardiovasculaire aux catécholamines- Respiratoire
o Hyperventilation, dyspnée- Métabolique
o Inhibition de la glycolyse anaérobie, réduction de la production d’ATP
o Hyperkaliémie- Cérébral
o Inhibition du métabolisme cellulaire
o Confusion et coma
Pour les acidoses métaboliques par excès d’acides inorganiques (cad les acidoses hyperchlorémiques et les acidoses par intoxication), avec ou sans insuffisance rénale sous-jacente, le traitement fait généralement appel à l’administration exogène de bicarbonate de sodium et à la correction de la cause lorsque cela est possible.
Le traitement des acidoses métaboliques par excès d’acides organiques est plus controversé quant à l’opportunité de l’administration de bicarbonate. Cette controverse tient au fait que l’anion organique accumulé est rapidement oxidé en bicarbonate lorsque la cause de l’acidose est corrigée.
Les risques d’une correction trop importante par du bicarbonate de sodium sont la survenue d’une alcalose métabolique par "rebond", l’élévation de la pCO2 tissulaire notamment chez les patients avec une fonction ventilatoire limite ou après arrêt cardiaque, et enfin l’hypernatrémie et la surcharge hydrosodée chez des patients avec une insuffisance cardiaque ou rénale sous-jacente (auxquels cas un traitement diurétique et/ou une hémofiltration peuvent être nécessaires).
Le bicarbonate de sodium doit être administré sous forme de perfusion intraveineuse. Il est recommandé de calculer la quantité de bicarbonate à administrer sur la base du déficit en bicarbonate et du volume de distribution présumé, soit en général : quantité HCO3 en mmol = d [HCO3-] x 0,5 x PDC (en kg). L’objectif est de remonter rapidement le pH sanguin au-dessus de 7,20 et la bicarbonatémie au-dessus de 10 mmol/l
2.3.2. Acidoses chroniques
Le traitement de ces acidoses chroniques d’origine rénale est impératif afin de prévenir ou de corriger la fonte musculaire (la protéolyse musculaire est stimulée par l’acidose métabolique et l’hypercortisolisme résultant), la lithiase rénale ou la néphrocalcinose, la déminéralisation osseuse et chez l’enfant le retard de croissance. Le traitement fait appel à l’administration de sels alcalins (bicarbonate ou citrate) de sodium ou de potassium selon le mécanisme de l’acidose.
P.S.
LECTURES RECOMMANDÉES :
Gluck SL. Acid-base. Lancet 1998 ;352:474
Adrogue HJ, Madias NE. Management of life-threatteneing acid-base disorders. NEJM 1998 ;333:26