|
|
|
|

|
|
OBJECTIFS
|
|
|
 |
PLAN DU CHAPITRE
|
|
|
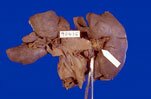
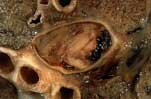
Le syndrome néphrotique est défini classiquement par une protéinurie supérieure à 3,5 g/j.1.73m2 de surface corporelle saccompagnant dune hypoalbuminémie inférieure à 30 g/l et dune hypoprotidémie inférieure à 60 g/l. De plus en plus dans la littérature internationnale, le syndrome néphrotique est défini par une protéinurie abondante supérieure à 3,5 g/24 h car la définition incluant lhypoalbuminémie et lhypoprotidémie est arbitraire et cest la protéinurie abondante par elle-même qui est associée à de nombreuses complications ou conséquences importantes sur le plan clinique.
 1. Causes de protéinurie néphrotique : 1. Causes de protéinurie néphrotique :
La néphropathie diabétique est actuellement la cause la plus fréquente de protéinurie néphrotique.
Plusieurs formes de maladie glomérulaire primitive peuvent rendre compte de la grande majorité des cas de syndrome néphrotique chez les sujets non diabétiques. La fréquence relative de ces maladies glomérulaires responsables de syndrome néphrotique varie selon lâge.
Tableau : Fréquence relative des maladies glomérulaires primitives au cours du syndrome néphrotique de lenfant et de ladulte.
| Maladie |
Enfant |
Adulte < 60 ans |
Adulte > 60 ans |
| LGM |
76 |
20 |
20 |
| HSF |
8 |
15 |
2 |
| GEM |
7 |
40 |
39 |
| GMP |
4 |
7 |
0 |
| Autres |
5 |
18 |
39 |
Le syndrome néphrotique idiopathique répond fréquemment au traitement par corticostéroïdes et peut se présenter soit sous la forme dune néphropathie glomérulaire à lésions glomérulaires minimes lorsque le glomérule apparaît normal en microscopie électronique mais présente des fusions des pédicelles en microscopie électronique ou encore sous la forme dune hyalinose segmentaire et focale. Il est possible mais encore controversé que ces deux formes représentent les deux extrêmes dun spectre de maladie au cours de laquelle la hyalinose segmentaire et focale est la forme la plus sévère et de mauvais pronostic progressant volontiers vers linsuffisance rénale.
Chez ladulte la cause la plus fréquente de syndrome néphrotique est la glomérulonéphrite extramembraneuse. La glomérulonéphrite membrano-proliférative est rare et la glomérulonéphrite à dépôts mésangiaux dIgA, la cause la plus fréquente de maladie glomérulaire nest que rarement responsable de syndrome néphrotique. Toutes les formes de néphropathie glomérulaire peuvent être associées aux cancerx (carcinome, sarcome, lymphome, leucémie) mais ceci doit être particulierement évoqué avec la glomérulonéphrite extramembraneuse et/ou chez des patients âgés. Il est également nécessaire de réaliser une immunoélectrophorèse des urines pour éliminer le myélome ou une amylose primitive rénale.
Le syndrome néphrotique peut être également causé par un grand nombre de maladies relativement plus rares. La néphropathie liée au HIV est responsable de protéinurie néphrotique et dinsuffisance rénale mais ceci est rarement la première manifestation clinique du SIDA. La prééclampsie est souvent associée à une protéinurie de rang néphrotique qui elle-même est associée à un risque accru de prématurité et dhypotrophie fStale mais qui ne comporte pas forcément un risque maternel plus mauvais.
Tableau : Causes rares de syndrome néphrotique
- Glomérulopathie fibrillaire
- Amylose
- Maladie des chaînes légères
- Eclampsie
- Maladies infectieuses
- bactérienne (glomérulonéphrite post-streptococcique, endocardite infectieuse, syphilis)
- virale (hépatite B, hépatite C, HIV)
- parasitaire (fièvre Quarte paludéenne, schistosomiase, filariose, toxoplasmose)
- Cancers (surtout associés aux glomérulonéphrites extramembraneuse, voire syndrome néphrotique à lésions glomérulaires minimes)
- Maladies systémiques (le plus souvent le lupus érythémateux systémique)
- Syndromes héréditaires (syndrome dAlport, syndrome onycho-patellaire)
- Allergies
- médicaments ( sels dor, D-pénicillamine, anti-inflammatoires non stéroïdiens, captopril, interféron-alpha)
- antigènes environnementaux (houx, piqûres de guêpe, antigène inhalé)
- drogue (héroïne).
|
 2. Physiopathologie de la fuite urinaire de protéines 2. Physiopathologie de la fuite urinaire de protéines
Le passage de protéines plasmatiques de poids moléculaire supérieur à 70 KD à travers la paroi capillaire glomérulaire est normalement restreint par une barrière sélective de charge ainsi quune barrière sélective de taille. La barrière sélective de charge résulte de la présence dun revêtement polyanionique de la membrane basale glomérulaire et des cellules avoisinantes qui restreint le passage de protéines plasmatiques polyanioniques de taille moyenne (environ 70 KD) principalement lalbumine. La barrière sélective de taille qui résulte de la présence de pores dans la membrane basale glomérulaire et dans les diaphragmes de fente épithéliale assure la restriction au passage (hindrance) des protéines plasmatiques de plus gros poids moléculaire au-dessus de 80KD.
Le syndrome néphrotique à lésions glomérulaires minimes résulte principalement dune perte de la sélectivité de charge alors que les autres glomérulonéphrites par exemple extra-membraneuses résultent essentiellement dune perte de la sélectivité de taille.
Le mécanisme de laltération glomérulaire aboutissant à lanomalie de perméabilité capillaire glomérulaire est variable. Chez les patients ayant une hyalinose segmentaire et focale récidivante après transplantation rénale, des interventions thérapeutiques qui adsorbent les immunoglobulines, comme le passage sur des colonnes dimmunoadsorption ou de protéines A entraînent une réduction considérable de la protéinurie. Un facteur plasmatique présumé produit par des lymphocytes augmente lexcrétion urinaire dalbumine chez des rats de rein perfusé. Ce facteur augmente la perméabilité à lalbumine de glomérules isolés et sa présence est associée à un taux important de récidive de la maladie après transplantation rénale.
 3. Conséquences cliniques de la protéinurie néphrotique 3. Conséquences cliniques de la protéinurie néphrotique
Le syndrome néphrotique saccompagne dune rétention hydrosodée aboutissant à la formation dSdèmes périphériques. On a longtemps pensé que cette rétention rénale de sodium résultait de ladaptation rénale à lhypovolémie liée à la baisse de la pression oncotique. Cette réponse rénale était considérée comme une réponse adaptée homéostatique à lhypovolémie médiée par lactivation des systèmes rénine-angiotensine , vasopressine et sympatique.
De nombreux éléments suggèrent une autre interprétation pour expliquer la rétention hydrosodée au cours du syndrome néphrotique. La plupart des patients ont en effet un volume plasmatique normal, voire augmenté et seuls les enfants avec un syndrome néphrotique à lésions glomérulaires minimes ont le plus souvent une hypovolémie. Laugmentation de pression artérielle pendant la phase de syndrome néphrotique est également en faveur dune hypervolémie. De même, la concentration de peptide atrial natriurétique est souvent augmentée, suggérant plutôt une hypervolémie. Le blocage pharmacologique du système rénine-angiotensine-aldostérone ninduit pas de natriurèse, comme cela serait attendu en cas dactivation compensatrice de ce système. Enfin, la rétention hydrosodée survient avant la survenue dune protéinurie massive et dune hypoalbuminémie au stade initial de la maladie. Inversement pendant la phase initiale de rémission, la natriurèse augmente avant la diminution de la protéinurie. Lensemble de ces éléments suggère une rétention primitive de sodium par le rein. Expérimentalement dans un modèle de syndrome néphrotique unilatéral, seul le rein exposé à un toxique podocytaire, la puromicine, développe une protéinurie et une rétention hydrosodée. Les études en microponction montrent également que la réabsorption sodée est augmentée surtout dans les sites distaux du néphron. Le mécanisme de rétention hydrosodée du syndrome néphrotique semble donc pouvoir être rapproché de celui opérant au cours des syndromes néphritiques au cours desquels linflammation glomérulaire est responsable dune rétention primitive de sel et dSdème avec hypervolémie mais sans diminution de lalbuminémie.
Le mécanisme rénal de rétention du sodium au cours du syndrome néphrotique reste mal connu. La rétention sodée est améliorée par la dénervation rénale. Certains éléments suggèrent également un défaut post-récepteur de la réponse au peptide atrial natriurétique.
Traitement de la rétention hydrosodée
La résolution du syndrome oedémateux ne peut être obtenue que si une balance sodée négative est induite. Pendant la phase de formation initiale de lSdème, lexcrétion sodée urinaire peut sabaisser jusquà 10 mmol/jour. Les apports en sodium alimentaire ne peuvent être réduits aussi bas, mais linduction dune balance sodée négative par les diurétiques est grandement facilitée si lapport sodé alimentaire est diminué aux alentours de 50 mmol/jour (environ 3 g de NaCl). En raison de lavidité du rein pour le sodium chez les patients avec syndrome néphrotique, des diurétiques de lanse puissants sont indispensables. En raison de sa courte durée daction, le furosémide peut être administré en 2 ou 3 doses quotidiennes. Des doses élevées sont souvent nécessaires car en plus de lavidité du rein pour le sodium, le furosémide et dautres diurétiques sont liés à lalbumine dans la lumière intratubulaire des patients avec protéinurie. La liaison à lalbumine est en compétition avec la liaison sur les protéines cibles, cest-à-dire les cotransporteurs du sodium.
LSdème doit être corrigé lentement. Une natriurèse trop rapide peut induire une hypovolémie qui peut être suffisamment sévère pour occasionner une insuffisance rénale aiguë, généralement fonctionnelle mais parfois organique par nécrose tubulaire en cas de choc hypovolémique. Le risque de survenue dune insuffisance rénale est augmenté par lutilisation des antiinflammatoires non stéroïdiens.
De plus, lhémoconcentration augmente le risque de complications thromboemboliques. Ladministration prophylactique dhéparine, danticoagulant et les bas de contension est donc indispensable.
La perfusion dalbumine à but dexpansion volémique ne doit être utilisée que dans les cas exceptionnels dhypotension symptomatique. Dans les autres cas, les perfusions dalbumine ne sont pas efficaces parce que lalbumine perfusée est rapidement éliminée dans lurine et peuvent même être dangereuses car laugmentation rapide de la pression oncotique peut provoquer une hypertension artérielle, voire un Sdème pulmonaire chez les patients déjà hypervolémiques. De plus, à moyen terme, laugmentation du passage des protéines filtrées contribue à laggravation des anomalies de perméabilité glomérulaire et à la toxicité tubulointerstitielle des protéines réabsorbées.
Les complications thromboemboliques représentent une des causes majeures de morbidité-mortalité au cours du syndrome néphrotique. La thrombose de la veine rénale est particulièrement fréquente chez les patients ayant une glomérulonéphrite extra-membraneuse (20 à 30 %). La thrombose des veines rénales est souvent asymptomatique et seulement 10 % des patients développent une symptomatologie clinique sous la forme de douleurs lombaires, dune hématurie macroscopique, dune augmentation de la taille du rein et une aggravation de la fonction rénale. Une autre complication grave est lembolie pulmonaire qui est souvent cliniquement asymptomatique et na une traduction clinique que chez 1/3 des patients. La thrombose profonde veineuse est également fréquente notamment chez ladulte. La thrombose veineuse peut survenir dans dautres lits vasculaires en particulier cérébral où elle est particulièrement grave. Chez ladulte avec un syndrome néphrotique, les thromboses artérielles sont moins fréquentes que les thromboses veineuses. Il existe cependant une augmentation du risque dévénement coronarien chez les patients néphrotiques : le risque relatif de survenue dun infarctus du myocarde est de 5.5 et celui de mort par thrombose coronaire de 2.8. Le rôle respectif de la dyslipidémie et de létat préthrombotique dans ces complications coronaires reste cependant à préciser.
Lincidence cumulative de complications thromboemboliques au cours du syndrome néphrotique est denviron 50 %. Il y a cependant peu de facteurs précis permettant de prédire le risque individuel mais globalement une hypoalbuminémie sévère inférieure à 25 g/l, une protéinurie abondante supérieure à 10 g/jour, une hyperfibrinogénémie, une concentration abaissée dantithrombine III à moins de 75 % de la normale et une hypovolémie y compris sous diurétiques sont significativement associées avec un excès de risque de complications thromboemboliques.
Tableau 3 : Principaux facteurs contribuant à létat dhypercoagulabilité au cours du syndrome néphrotique
- Baisse des facteurs IX et facteur XI
- Augmentation des facteurs procoagulants, facteur V, facteur VIII
- Augmentation du fibrinogène
- Diminution des inhibiteurs de la coagulation : antithrombine III
- Altération du système fibrinolytique (augmentation de lalpha 2 antiplasmise, plasminogène diminué
- Augmentation de lagrégabilité plaquettaire (thrombocytose, augmentation de la libération in vitro des pro-agrégants, augmentation du facteur IV et de la béta-thromboglobuline in vivo
- Altération de la fonction endothéliale
|
Le bénéfice dune anticoagulation prophylactique chez les patients atteints de glomérulonéphrite extramembraneuse a été évalué par analyse de décision. Une anticoagulation prophylactique comporte moins de risque quun traitement anticoagulant adapté après survenue dune complication thromboembolique. Le traitement anticoagulant prophylactique doit être administré tant que lalbuminémie est inférieure à 20 g/l ou la protéinurie reste néphrotique.
Tant chez les patients avec un syndrome néphrotique dautre nature quune glomérulonéphrite extramembraneuse, une anticoagulation prophylactique doit être considérée seulement si le risque thrombotique est élevé. Lanticoagulation est par contre impérative lorsquune complication thromboembolique a été mise en évidence. Chez ces patients, lhéparine doit être administrée quoique son effet soit atténué en raison de la diminution de la concentration dantithrombine III (dont la fuite urinaire est grosso modo parallèle à celle de lalbumine). En cas dembolie pulmonaire, un traitement thrombolytique par urokinase intraveineuse peut être administré.
Le mécanisme de létat hypercoagulable ou préthrombotique au cours du syndrome néphrotique est multifactoriel. Les concentrations ou lactivité de nombreux facteurs sont anormaux (voir tableau 3).
Antérieurement, en labsence de traitement, de nombreux enfants ayant un syndrome néphrotique mourraient dinfection bactérienne, notamment de péritonite à pneumocoque. Cette complication est devenue rare mais linfection continue à être un problème chez les patients recevant des traitements immunosuppresseurs et chez lesquels les infections virales sont fréquentes. La susceptibilité aux infections bactériennes est attribuée à une diminution de la concentration dIgG ou des facteurs alternes du complément, comme le facteur B. La vaccination antipneumococcique peut être utilisée de façon prophylactique.
Lhyperlipidémie représente un facteur de risque important de maladie cardiovasculaire. Au cours du syndrome néphrotique, il existe une augmentation variable de la concentration des lipoprotéines de très basse densité VLDL, des lipoprotéines de densité intermédiaire IDL et des lipoprotéines de faible densité LDL, ce qui aboutit à une élévation de la concentration sérique totale de cholestérol isolée ou associée à une augmentation de la concentration sérique de triglycérides. La fraction HDL des lipoprotéines est habituellement normale. De plus, la lipoprotéine Lp(a) est augmentée quels que soient les isoformes dApo A et cette augmentation est corrigée après rémission du syndrome néphrotique ou après traitement symptomatique antiprotéinurique.
Deux mécanismes contribuent à la dyslipidémie du syndrome néphrotique : (1) une hyperproduction et (2) une diminution du catabolisme des lipoprotéines contenant des Apo-B. Le mécanisme pathologique est différent chez les patients ayant une hypercholestérolémie isolée et ceux ayant une hypercholestérolémie et une hypertriglycéridémie combinée. Le catabolisme des chylomicrons et des VLDL est diminué au cours du syndrome néphrotique. Le catabolisme fractionnel des Apo-B LDL est abaissé chez les patients ayant une hypercholestérolémie isolée et élevé chez les patients avec une hyperlipidémie combinée. Lhypoalbuminémie et la baisse de la pression oncotique pourraient jouer un rôle car lélévation de la pression oncotique par linjection de dextrans corrige partiellement lhyperlipidémie. Dautres mécanismes entrent en jeu car les modifications lipidiques chez les animaux néphrotiques ne sont pas reproduites entièrement chez les rats analbuminémiques. Une relation causale entre les anomalies de la perméabilité glomérulaire et les anomalies du métabolisme lipidique est vraisemblable : une glycoprotéine acide alpha 1 retrouvée dans lurine des patients néphrotiques corrige les altérations de la lipolyse. Il est donc probable que le catabolisme anormal des lipoprotéines résulte au moins en partie de la perte urinaire de certaines substances régulatrices du métabolisme lipidique.
En raison des effets de la dyslipidémie sur le risque cardiovasculaire et peut être sur la progression de la maladie rénale, un traitement est souhaitable quoiquil ny ait pas détude contrôlée disponible. Des interventions non pharmacologiques sont utiles par exemple les régimes à base de protéine de soja diminuent significativement la cholestérolémie, le LDL cholestérol et lApo lipoprotéine B alors quil ny a pas de modification de la triglycéridémie. Les traitements à base dhuile de poisson diminuent les triglycérides et les VLDL mais augmentent le LDL-cholestérol. Les statines permettent une diminution denviron 30 % du cholestérol total et du LDL cholestérol. Les inhibiteurs de lenzyme de conversion en diminuant la protéinurie réduisent également les concentrations du cholestérol total et de LDL cholestérol.
De nombreuses protéines de liaison sont éliminées dans lurine au cours du syndrome néphrotique. En conséquence les concentrations plasmatiques de nombreux ions (fer, cuivre, zinc), vitamines (métabolites de la vitamine D), hormones (hormones thyroïdiennes et stéroïdiennes) et médicaments sont abaissées parce que les concentrations de ligands (protéines de liaison) sont réduites. La perte urinaire des protéines de liaison semble, au moins dans le cas de la vitamine D, être responsable dune déplétion des ligands. De nombreux médicaments sont liés à lalbumine. Lhypoalbuminémie diminue le nombre de sites de liaison disponibles et augmente donc la fraction de médicament libre actif circulant. En état déquilibre, ceci est contrebalancé par un métabolisme plus rapide. Des concentrations plus élevées de médicament libre actif peuvent devenir toxiques, comme cela a été montré avec la prednisolone et peut être les coumariniques. Lorsque les concentrations plasmatiques totales de ces médicaments sont mesurées, une concentration abaissée de médicament fortement liée aux protéines nindique pas nécessairement une concentration efficace basse. La concentration de médicament libre peut être normale, voire élevée. Des considérations analogues sappliquent aux hormones liées aux protéines, comme les hormones thyroïdiennes et stéroïdiennes.
 4. Traitements du syndrome néphrotique 4. Traitements du syndrome néphrotique
Une protéinurie abondante et persistante constitue le principal prédicteur dune progression rapide vers linsuffisance rénale terminale. Cette relation est causale et pas seulement épidémiologique si bien que la réduction de la protéinurie constitue en soi un but thérapeutique.
4.1.1. Les inhibiteurs de lenzyme de conversion permettent de réduire la protéinurie et sont indiqués même chez des patients normotendus. Il existe une dissociation temporelle entre les effets hémodynamiques et antiprotéinuriques des inhibiteurs de lenzyme de conversion. Leffet antiprotéinurique peut mettre plusieurs semaines à se manifester et il est donc plus tardif que leffet hypotenseur. Leffet antiprotéinurique est partiellement indépendant des effets sur la baisse de la pression artérielle. Une réduction de la protéinurie peut même être observée en labsence de tout effet sur la pression artérielle. La réponse antiprotéinurique pourrait être partiellement déterminée par le génotype ACE mais ce point reste controversé. Surtout leffet antiprotéinurique dépend de la balance sodée et peut être augmenté par un régime sans sel ou un traitement diurétique et également semble-t-il par un régime restreint en protéines.
4.1.2. Les anti-inflammatoires non stéroïdiens permettent de réduire la protéinurie de façon proportionnellement plus importante quils nabaissent la filtration glomérulaire. En raison des effets indésirables considérables sur laggravation de la fonction rénale et la tolérance gastro-intestinale, cette approche nest pas recommandée.
4.1.3. Les régimes restreint en protéines ne permettent pas dobtenir une réduction importante et constante de la protéinurie par opposition aux inhibiteurs de lenzyme de conversion. Une réduction de la protéinurie et surtout des modifications lipidiques favorables ont été observées avec un régime restreint en protéines, composé de protéines de soja (environ 0,7 g de protéines/kg/jour). Le risque principal de ces régimes restreints en protéines est la dénutrition qui représente lun des prédicteurs de risque les plus importants de mortalité au cours de linsuffisance rénale terminale. Ces régimes restrictifs sont peu utilisés et ne peuvent se faire quen milieu spécialisé sous surveillance nutritionnelle rigoureuse.
Des interventions immunologiques spécifiques ne sont disponibles que pour certaines causes de syndrome néphrotique. La colchicine prévient ainsi la progression de latteinte rénale amyloïde des patients avec une fièvre familiale méditerranéenne. Le traitement par interféron alpha avec ou sans lamuvidine permet de corriger ou daméliorer le syndrome néphrotique associé à lhépatite B, la glomérulonéphrite membrano-proliférative associée à lhépatite C et la cryoglobulinémie associée à lhépatite C. Le traitement dinfection responsable de syndrome néphrotique, comme lhydatidose, larrêt de médicament responsable de syndrome néphrotique médicamenteux et la chimiothérapie ou lexérèse de tumeur au cours de syndrome néphrotique associé aux néoplasies permettent généralement de corriger les anomalies urinaires.
Dans tous les autres cas, des interventions immunitaires non spécifiques restent la seule option disponible sauf si la fonction rénale est sévèrement altérée (créatinine plasmatique > 177 µmol/l) auquel cas le traitement immunosuppresseur comporte un risque de toxicité trop important .
Chez ladulte, la biopsie rénale est une étape indispensable avant denvisager tout traitement immunosuppresseur. En effet, le traitement immunosuppresseur à laveugle nest pas dénué de risque et un traitement de courte durée insuffisant na que peu de chance daboutir à une réponse thérapeutique. Inversement, la biopsie rénale avec guidage echographique est un geste relativement dénuée de risque dans des mains entraînées. Cet examen confirme le diagnostic et apporte des informations pronostique importantes par la présence ou non dune fibrose tubulo-interstitielle.
Il ny a pas de consensus concernant le traitement des différentes variétés de syndrome néphrotique.
Chez ladulte avec un syndrome néphrotique à lésions glomérulaires minimes, un traitement par corticoïdes sur la base de prednisolone 1 mg/kg/jour est généralement entrepris pendant au moins 8 semaines et parfois plus longtemps chez certains patients particuliers. En labsence de réponse ou en cas de récidive fréquente ou en cas de dépendance vis-à-vis des corticoïdes, le cyclophosphamide 1 à 2 mg/kg/jour pendant une période de 8 semaines peut être tenté notamment si le patient est symptomatique ou présente des facteurs de risque de progression rénale (homme, hypertension, tabac, insuffisance rénale, protéinurie massive ou fibrose interstitielle). Une surveillance rigoureuse, notamment du compte leucocytaire et des plaquettes doit être effectuée et une contraception efficace doit être assurée chez la femme.
Pour les patients avec une hyalinose segmentaire et focale, une approche thérapeutique analogue peut être envisagée mais avec un taux de réponse nettement inférieur. Pour les patients qui ne répondent pas à ces premiers traitements, la cyclosporine peut être envisagée à condition de ne pas dépasser des doses de 5 mg/kg et de surveiller les concentrations plasmatiques résiduelles. La cyclosporine doit être évitée lorsquil existe une insuffisance rénale et/ou une fibrose interstitielle importante sur la biopsie rénale en raison du risque daggravation lié à la toxicité rénale propre de ce médicament. Il est important de prendre en compte quune hypercholestérolémie sévère interfère avec lefficacité de la cyclosporine. Dautre part, les lésions glomérulaires sous ce traitement continuent à progresser malgré la réduction de la protéinurie. Il faut de plus prendre en compte la toxicité rénale à long terme de ce traitement surtout compte tenu du fait que leffet antiprotéinurique nest que suspensif, ce qui nécessite souvent des traitements prolongés. En labsence de réponse thérapeutique au cours des 3 premiers mois de traitement, le traitement est inefficace et doit être interrompu.
Chez les patients avec une glomérulonéphrite extra-membraneuse pour laquelle une cause secondaire a été exclue, qui est symptomatique et à haut risque de progression, un traitement immunosuppresseur peut être tenté. Une combinaison de corticoïdes et dun cytotoxique, cyclophosphamie ou chlorambucil peut être tentée pendant une période ne dépassant pas 6 mois. En cas déchec un traitement par cyclosporine semble également efficace chez certains patients sélectionnés.
|
|
LECTURES RECOMMANDÉES
Orth S, Ritz E. The nephrotic syndrome. New Engl J Med 1998;338:1202
|
|
TEXTES COMPLÉMENTAIRES DANS LE SITE
|
|
Mise-à-jour : vendredi 5 mai 2000
Copyright © Tous Droits Réservés pour le site entier Nephrohus 2000
|
|
|
|